투여 방식 개량해 가격 높일 수 있어
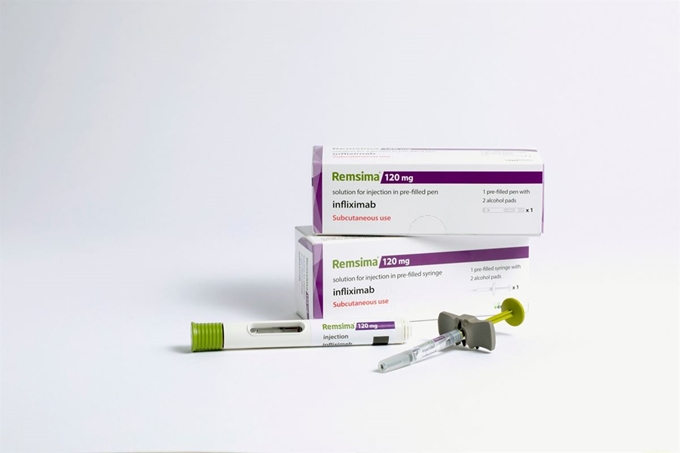
셀트리온의 바이오시밀러(바이오의약품 복제약) ‘램시마’가 주사하기 간편한 형태로 제형을 바꿔 ‘램시마SC’라는 이름으로 유럽에서 새롭게 출시된다.
셀트리온은 램시마SC가 지난 25일(현지시간) 유럽의약품청(EMA)에서 판매 허가를 받았다고 26일 밝혔다. 지난해 11월 EMA에 램시마 SC 판매 허가를 신청한 지 12개월 만이다.
램시마는 환자의 손등이나 팔목, 팔꿈치 안쪽 핏줄에 주삿바늘을 꽂는 정맥주사 형태다. 이와 달리 램시마SC는 위팔이나 허벅지에 바로 주삿바늘을 넣는 피하주사 방식으로 투여된다. 환자 입장에선 병원에서 오랜 시간을 보낼 필요가 없는 피하주사 형태가 삶의 질 측면에서 훨씬 긍정적이다.
램시마는 오리지널 바이오의약품인 다국적제약사 존슨앤존슨의 ‘레미케이드’(성분명 인플릭시맙)를 복제한 바이오시밀러다. 램시마SC는 바이오시밀러가 아닌 ‘바이오베터’로서 승인 절차를 밟았다. 바이오베터는 기존 바이오의약품이나 바이오시밀러의 효능이나 투여 방식 등을 개량해 가치를 높인 약을 말한다. 기존 제품들로 시장성이 입증된 데다 개량으로 가격을 더 높일 수 있어 제약사 입장에선 전통적인 신약개발보다 사업 위험성이 적다.
램시마의 치료 대상인 자가면역질환 분야에선 휴미라(제조사 애브비)와 레미케이드, 엔브렐(암젠) 등 3개 ‘블록버스터’ 의약품이 세계 시장을 이끌고 있다. 시장 규모가 50조원에 이른다. 셀트리온은 이들 약에 내성을 보이는 환자들이 램시마SC를 쓸 것으로 보고 있다. 이 시장이 약 10조원 규모가 될 거라고 셀트리온은 예상하고 있다.
램시마와 성분이 동일한 약 가운데 피하주사 제형은 램시마SC가 처음이다. 이에 셀트리온은 램시마SC를 기존 약보다 더 높은 가격에 판매하는 ‘프라임 시밀러’ 전략을 구사한다는 계획이다. 그만큼 수익성 향상도 기대하고 있다.
또한 셀트리온은 램시마SC 제형에 대해 130여개국에 특허를 출원했다. 특허 절차가 완료되면 향후 20여년 동안 해당 성분의 피하주사 시장을 독점할 수 있을 것으로 셀트리온은 내다보고 있다.
셀트리온 제품의 해외 유통과 마케팅을 담당하는 셀트리온헬스케어는 주요 유럽 시장에 갖춰 놓은 지점과 직판망을 통해 램시마SC를 직접 판매할 계획이다. 2020년 2월 독일을 시작으로 순차 출시해 내년 연말까지 유럽 전역으로 램시마SC 판매를 확대할 예정이다.
임소형 기자 precare@hankookilbo.com
기사 URL이 복사되었습니다.


댓글0