셀트리온·녹십자 코로나19 약 상용화 가속도
항체치료제, "내년 상반기 임상 종료 목표"
혈장치료제, "임상 1상 뛰어넘고 2상부터"

셀트리온의 인천 송도공장에서 임상시험에 쓰일 항체치료제가 제조되고 있다. 셀트리온은 이를 건강한 사람에게 투여하는 임상시험을 며칠 내 시작할 예정이다. 셀트리온 제공
셀트리온과 녹십자의 신종 코로나바이러스 감염증(코로나19) 치료제 개발에 속도가 붙고 있다. 셀트리온은 지난 17일 식품의약품안전처에서 임상시험 1상을 허가 받은 항체치료제 후보물질을 이번 주 중 피험자에게 투여할 예정이다. GC녹십자는 18일부터 임상시험용 혈장치료제 생산에 들어갔다.
서정진 셀트리온 회장은 20일 오전 온라인 기자간담회를 열고 “건강한 사람 32명에게 금주 중 항체치료제를 투여하는 임상 1상을 시작한다”고 밝혔다. 임상 1상은 한 달에서 한 달 반 정도 걸릴 것으로 예상된다. 이후에는 경증과 중증 코로나19 환자 200~300명을 대상으로 2상, 2,000~3,000명 대상으로 3상 임상시험을 우리나라와 유럽에서 진행할 계획이다. 서 회장은 “내년 상반기까지 임상 종료가 목표”라며 “2상 결과에서 효능과 안전성에 문제가 없다고 판단되면 식약처에 긴급사용승인을 요청하는 것도 고려 중”이라고 말했다. 긴급사용승인은 긴급히 필요하거나 대체제가 없는 신약에 대해 임상시험이 모두 끝나지 않았어도 예외적으로 허가를 내주는 제도다.
신속한 상업화를 위해 셀트리온은 오는 9월부터 인천 송도공장에서 항체치료제 상업생산에 돌입할 예정이다. 허가 직후 즉시 판매가 가능하도록 대비하면서 보급 가능한 생산량과 적정 가격도 파악하기 위해서다. 항체는 암이나 류마티스관절염 등 다른 질병에서 이미 여러 종류가 치료제로 사용돼왔다. 때문에 자사의 코로나19 항체치료제도 중대한 부작용은 없을 것으로 셀트리온 측은 기대하고 있다. 이번에 허가 받은 항체치료제 역시 동물실험(페럿, 햄스터, 원숭이)으로 효능과 안전성이 어느 정도 확보됐다는 설명이다.
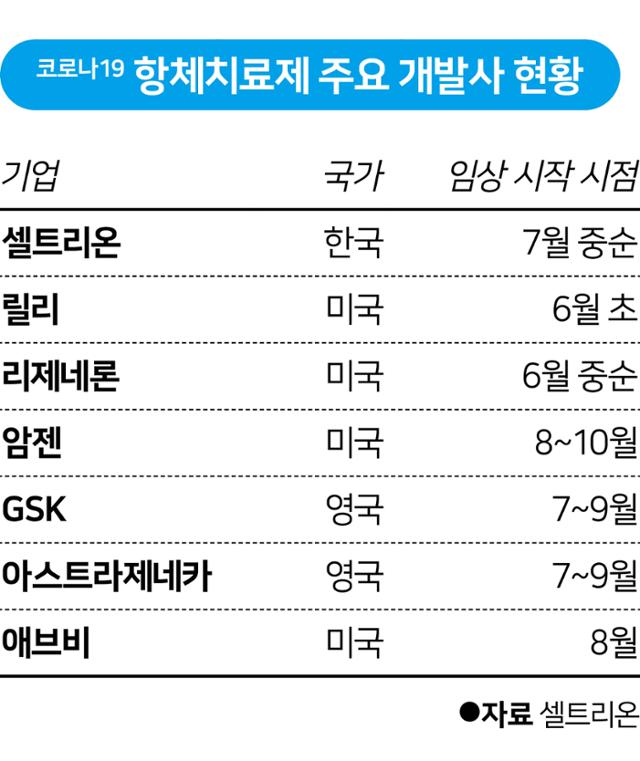
문제는 가격이다. 서 회장은 “효능이 좋고 부작용이 적은 항체치료제를 얼마나 많이, 저렴하게 보급할 수 있느냐가 가장 큰 숙제”라며 “개발비와 제조원가를 낮춰 어느 회사보다도 저렴하게 항체치료제를 공급하겠다”고 약속했다. 현재 각국에서 코로나19 항체치료제를 개발하고 있는 기업은 셀트리온을 포함해 51개다.

충북 청주에 있는 GC녹십자 오창공장에서 한 직원이 혈장치료제 제조 설비를 살펴보고 있다. 이곳에선 이달 18일부터 임상시험용 혈장치료제 생산이 시작됐다. GC녹십자 제공
다른 질병의 약을 활용하는 ‘약물 재창출’ 방식을 제외하면 코로나19 치료 약에선 현재 항체치료제와 혈장치료제가 개발이 가장 빠르다. 항체치료제는 다양한 종류의 항체 가운데 코로나19 바이러스가 세포 안으로 침투하지 못하도록 방해하는 능력이 뛰어난 것을 선별해 만든다. 혈장치료제는 코로나19에 걸렸다가 완치된 사람의 혈장(혈액 중 세포를 뺀 액체 성분)을 농축해 제조하는데, 여기엔 코로나19 바이러스를 기억하고 있는 항체가 다량 들어 있다.
GC녹십자는 지난 18일 충북 청주 오창공장에서 임상시험용 코로나19 혈장치료제 생산을 개시했다. 20일 오전 기준 총 1,032명이 치료제 개발을 위해 혈장을 기증하겠다는 의사를 밝혔고, 이 중 642명에게서 채혈이 완료됐다고 GC녹십자 측은 설명했다. 혈장치료제는 이미 중증급성호흡기증후군(SARS·사스), 중동호흡기증후군(MERS·메르스) 때 치료 효과가 확인됐기 때문에 임상 1상이 면제됐고 2상부터 진행될 예정이다. 항체치료제보다 개발 속도가 좀 더 앞서 있다.GC녹십자는 이달 마지막 주 식약처에 혈장치료제 임상시험을 신청할 예정이다. 김진 GC녹십자 의학본부장은 “혈장치료제가 빠른 시일 안에 의료현장에서 사용될 수 있도록 노력하겠다”고 말했다.
기사 URL이 복사되었습니다.


댓글0