
의약품 포장에 들어있는 환자용 의약품 첨부문서 내용이 형식적이라 실효성이 떨어진다는 비판이 나왔다. 내용이 자세하지 않고 전문용어가 많다는 지적이다. 의약품 첨부문서는 의약품을 안전하고 효과적으로 사용하기 위해 필요한 정보를 담은 문서로 의약품 제조사가 작성하고, 통상 의약품 포장 안에 포함돼 약과 함께 제공된다.
12일 한국보건사회연구원의 ‘의약품 첨부 문서의 국가별 운영 현황과 시사점’ 보고서에 따르면 국내와 달리 미국이나 유럽연합(EU) 등지에서는 의약품 첨부문서는 의약품 시판 허가 조건이다. 한국의 경우 약사법 58조에 첨부문서에 용법과 용량 등을 적시하도록 돼 있지만 구체적으로 어떤 내용이 포함돼야 하는지는 빠져 있다. 반면 일본의 경우 정부 가이드라인을 통해 △효능과 효과 △약효와 약리 △과도한 용량을 사용했을 경우 대응 방법 △약의 직경, 두께, 무게, 색깔, 식별코드 등을 표시하도록 하고 있다. 또 미국에서는 한국과 달리 외래 조제 시 반드시 환자에게 첨부문서를 전달하도록 하고 있다.

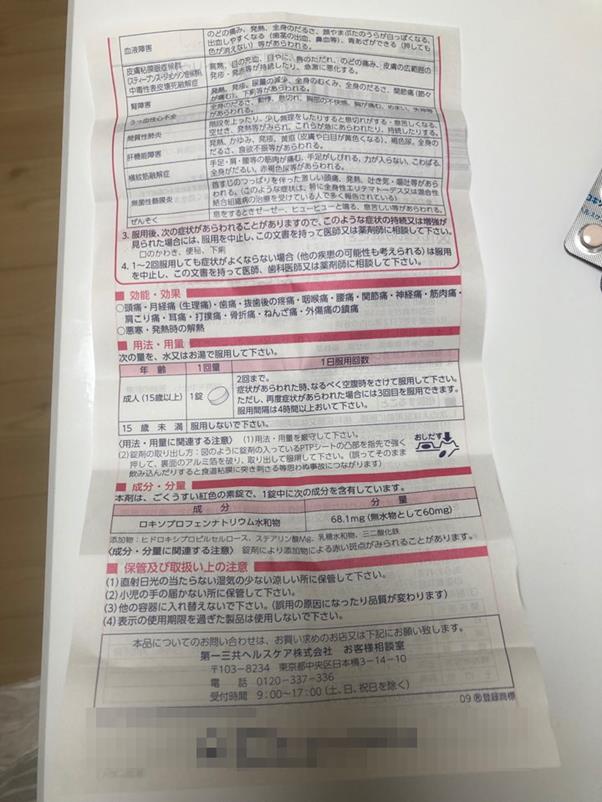
실제로 일본과 한국의 진통제 의약품 첨부문서를 비교해보면 일본 첨부문서는 한국보다 크기가 크고 붉고 두꺼운 괘선 테두리로 경고 등의 내용을 강조하고 있다. 내용도 구체적이다. 예컨대 부작용 부분을 보면 일본의 경우 ‘복용 후 다음의 상태가 나타날 경우 부작용의 가능성이 있으니 즉시 부작용을 중지하고 이 문서를 가지고 의사에게 약에 대해 상담하시오’라고 명시한 이후 소화관 출혈 등의 부작용을 예로 들고 있다. 소화관 출혈의 증상으로 △검은 대변 △복통 △구토 등을 병기해 부작용을 구체적으로 설명했다. 반면 한국의 경우 첨부문서에선 전문용어와 함께 ‘장기간 또는 과량 투여 시 전신 부작용으로 구역, 위장관 불쾌감, 호흡곤란 등이 나타날 수 있습니다’정도로 소략하게 돼있다. 다만 일본은 정부가 지정한 일부 의약품만 환자용 첨부문서를 제공한다.
박실비아 보사연 연구위원은 보고서에서 “(한국도) 허가당국이 첨부문서에 대한 감독 의무와 권한을 가져야 한다”면서 “첨부문서의 이해도와 가독성을 높이고 첨부문서가 반드시 환자에게 전달되도록 기전(제도)를 만들어야 한다”라고 주장했다.
김민호 기자 kmh@hankookilbo.com
기사 URL이 복사되었습니다.

댓글0