
사람과 동물간 이종이식에서부터 자폐증 치료까지.
‘유전자 편집’(Genome Editing) 기술이 인류의 생명 연장을 향한 연구를 거듭 진보시키고 있다. 특히 미국과 중국 등의 저명한 과학자들이 올 들어 ‘유전자 가위’기술을 활용한 연구 성과를 쏟아내면서 과학계는 기대감을 키우는 중이다. 유전자를 자르고 붙이는 특정 화학 물질을 뜻하는 유전자 가위는 유전자의 잘못된 부분을 잘라 없애 수술이나 약물치료가 불가능한 질환들을 고쳐준다.
하지만 인간과 동물을 고통에서 해방시킨다는 이 기술이 무분별하게 사용되면 생명체를 조작하는 비극을 낳을 것이란 우려의 시선 역시 늘어나고 있다. 유전자 가위 기술이 본격적으로 활용된 지 겨우 10년여밖에 안 된 데다, 연구 도중 부작용도 적잖게 나타나 기술 적용에 속도 조절이 필요하다는 지적이다.
올 한 해 유전자 편집 연구 성과 잇따라
BBC 등 외신은 12일 미국 하버드대 연구진이 돼지 장기로부터 인간 이식에 부적합한 유전자 일부를 제거하는 데 성공, 사람과 돼지간 이종이식의 길이 열렸다고 보도했다. 연구진을 이끄는 조지 처치 유전학박사는 유전자 가위 ‘크리스퍼’ (CRISPR/cas9)를 이용해 내인성 레트로바이러스 DNA 염기서열을 잘라냈는데, 세포들이 이후에도 살아있는 것을 발견했다. 돼지의 심장판막은 인간의 심장판막을 대체하는 데 일부 사용되고 있지만, 조직 속 바이러스 탓에 돼지 장기를 통째로 이식하지는 못한다.
처치 박사는 특히 염기서열을 6개까지 밖에 제거하지 못한 최근까지의 연구들에서 나아가 한 번에 62개의 PERV 염기서열을 잘라내는 성과를 냈다. 그는 “크리스퍼 가위가 동물의 어떤 유전자든 교정할 수 있다는 것이 입증됐다”며 “돼지 장기를 사람에 이식하는 이종이식의 저변이 확대된 셈”이라고 밝혔다.
지난달 30일 과학학술지 네이처에는 중국의 베이징유전체학연구소(BGI)가 유전자 교정 기술을 이용해 애완용 미니 돼지를 개발했다는 연구가 실리기도 했다. BGI가 개발한 미니 돼지는 완전히 성장해도 무게가 15㎏ 밖에 되지 않아 중형 애완견과 덩치가 비슷하다. 보통 돼지(60~100㎏)보다 몸집이 작은 바마 돼지(35~50㎏)의 유전자를 교정한 성과다. BGI는 돼지 태아에서 떼어낸 세포의 성장 호르문 수용체 유전자 중 하나를 유전자가위 ‘탈렌’을 통해 잘라내 성장을 막았다.
네이처에 따르면 미니 돼지는 중국 시장에서 한 마리당 1만위안(약 180만원) 정도에 판매될 예정이다. 소비자들은 돼지의 털 색깔이나 무늬를 선택해 따로 주문해 구입할 수도 있다. 리용 BGI 연구소장은 중국 선전에서 열린 ‘선전국제바이오테크리더십 서밋’에서 미니 돼지를 공개하고 “수요가 얼마나 되는지 조사하고 있다”면서 “1만위안으로 가격을 책정한 것은 시장 수요를 지켜보기 위한 것”이라고 밝혔다. 과학계에선 유전자 가위 기술로 만든 동물이 시장에서 판매되는 첫 사례인 만큼 주목하고 있다.
올 6월에는 네이처에 김진수 기초과학연구원(IBS) 유전체교정연구단장과 인시준 중국 옌볜대 교수 공동 연구진이 유전자 편집 기술을 통해 일반 돼지보다 근육량이 많은 슈퍼돼지(이중근육 돼지)를 만들었다는 연구가 발표됐다. 이들 역시 ‘탈렌’을 이용해 돼지의 체세포에서 근육의 성장을 억제하는 유전자 ‘마이오스타틴’을 떼 내 기능을 발휘하지 못하도록 했다.
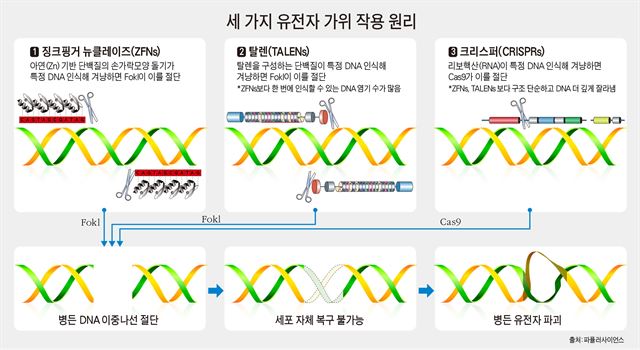
유전자 가위 연구 역사 불과 10여년
유전자 연구의 중심이 된 ‘유전자 가위’가 실제 연구에 활용된 지는 10년이 조금 넘었다. 1세대 유전자 가위 ‘징크 핑거 뉴클레이즈’(ZFNsㆍZinc Finger Nucleases)는 1980년대 중반 발견됐지만 2003년 들어서야 유전체 교정에 사용되기 시작했다. 그로부터 8년여 뒤인 2011년 말 1세대 유전자 가위의 단점을 개선한 2세대 ‘탈렌’(TALENsㆍ Transcriptor Activator-Like Effector Nucleases)이 발표됐지만 제작이 어려워 연구 적용은 쉽지 않았다.
2013년 초에 들어서 유전자 교정의 혁명을 가져다 준 기술로 평가 받는 ‘크리스퍼’가 개발됐다. 세균은 바이러스의 침입을 받으면 그 DNA 조각을 자신의 유전체에 삽입해 두는데, 이를 크리스퍼라고 한다. 과학자들은 크리스퍼에서 작은 리보핵산(RNA)이 만들어지고 이것이 Cas9라는 단백질과 결합한다는 사실을 알아냈다. 바이러스가 다시 침입하면 RNA가 바이러스 DNA를 찾아내 결합한 다음 Cas9가 이를 잘라내 바이러스가 복제하는 걸 차단하게 된다.
크리스퍼 가위는 1, 2세대 유전자 가위와 달리 복잡한 단백질 구조가 없고 DNA 절단 정도도 더욱 깊어 연구에 적극 활용되고 있다. 하지만 이전 세대 가위들과 달리 보호장치가 없어 자칫 잘못하면 목표 유전자 이외의 것을 잘라내 돌연변이를 일으킬 수 있다는 치명적 단점이 있다.
인간 배아 연구 확대에 논란 격화
유전자 가위 기술이 등장한 지 얼마 되지 않은 데다 한계도 뚜렷하다는 지적이 잇따르면서 연구 확대를 두고 목소리가 엇갈린다. 미 하버드의대 생명윤리학자 진타인 룬쇼프는 “동물의 생리학적 한계를 넓히려는 시도는 동물뿐 아니라 인간에게도 적용돼 적잖은 부작용을 낳을 것”이라고 우려했다. 네이처도 지난 6월 30일 ‘슈퍼돼지’ 소식을 보도하면서 “기존 32마리 돼지 중 13마리만 8개월 동안 생존했다”며 “2마리는 여전히 살아 있지만 그 중 한 마리만 건강한 것으로 보인다”고 전했다.
특히 올 초 인간 배아를 이용한 유전자 교정 연구까지 등장하면서 논란은 격화하고 있다. 중국 광둥(廣東)성 광저우(廣州) 중산대 황쥔주 박사팀은 지난 4월 온라인과학저널 프로테인앤셀을 통해 폐기된 인간 배아를 통해 유전자 교정 연구 성과를 발표했다. 이들은 지중해성빈혈을 유발하는 유전자를 교정하기 위해 총 86개 수정란에서 관련 유전자를 잘랐지만, 48시간 이후 생존한 71개 수정란 중 28개 유전자만 원하는 대로 바뀌어 성공률 32.6%를 달성하는 데 그쳤다. 또 목표로 한 유전자 외에 의도하지 않은 유전자를 잘라버리는 돌연변이의 발생 비율도 높았다. 연구진 스스로도 “정상적인 배아에 유전자 교정을 적용하려면 성공률이 100%에 근접해야 한다”며 “인간 배아에 유전자 교정을 적용하는 것은 아직 시기상조”라고 밝혔다.
이러한 우려에도 불구하고 전 세계 과학자들의 인간 배아를 통한 유전자 교정 연구 시도는 계속되고 있다. 지난 18일에는 영국 프란시스크릭연구소가 자국의 인공수정배아관리국(HFEA)에 “인간 배아를 이용한 연구를 허락해달라”며 연구 승인을 신청했다. 이 연구소는 DNA 복구 원리를 밝혀내 올해 노벨화학상을 탄 토마스 린달 교수가 속해 있는 곳이다. 연구소는 “연구 목표는 인간 배아가 제대로 발달하는 데 필요한 유전자들이 무엇인지 이해하려는 것”이라며 “다양한 유전 질환을 지료하기 위해 필수적인 연구이기도 하다”고 밝혔다. 가디언은 HFEA 위원회에서 실험이 정당하다고 인정되면 14일 내 파기한다는 조건으로 배아 연구를 허용하는 법률에 의거해 승인될 가능성이 있다고 전했다.
미 미네소타대 유전학자인 다니엘 보이타스 박사는 네이처에 “이 기술에 대한 안전과 윤리 기준이 전혀 마련돼 있지 않은 상태”라면서 “연구가 활발한 각국에서뿐만 아니라 전 세계 과학계가 적절한 규제 프레임을 설정하고 이 기술의 잠재력과 위험성에 대해 논의하는 기회가 필요하다”고 밝혔다.
신지후기자 hoo@hankookilbo.com
기사 URL이 복사되었습니다.


댓글0